大塚メディカルデバイス/大塚製薬:Paradise 超音波式腎デナベーションシステム 治療抵抗性高血圧症を適応症に保険適用、販売開始
東京--(BUSINESS WIRE)-- (ビジネスワイヤ) -- 大塚メディカルデバイス株式会社(本社:東京都、代表取締役社長:東條紀子、以下「大塚メディカルデバイス」)および大塚製薬株式会社(本社:東京都、代表取締役社長:井上眞、以下「大塚製薬」)は、治療抵抗性高血圧症を適応症とする大塚メディカルデバイスの医療機器「Paradise™ 超音波式腎デナベーションシステム (Paradise システム)」が、3月1日に保険適用されたことをお知らせします。これに伴い、大塚メディカルデバイスは、3月2日よりParadise システムの販売を開始し、大塚製薬と共同プロモーションを行います。
本プレスリリースではマルチメディアを使用しています。リリースの全文はこちらをご覧ください。:https://www.businesswire.com/news/home/20260301067557/ja/
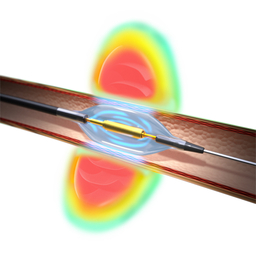
 Paradise カテーテル
Paradise カテーテル
Paradise システムは、大塚メディカルデバイスの米国子会社であるRecor Medical, Inc.(以下「Recor Medical」)が開発した医療機器です。本システムは、利尿薬を含むクラスの異なる3剤を使用しても血圧が目標値まで下がらない治療抵抗性高血圧症の患者さんを対象としています。腎交感神経の過活動を抑制することで血圧降下を目指す新たな治療法である超音波式腎デナベーションを、国内で初めて提供するものです。
今回の保険適用により、治療抵抗性高血圧症に対する新たな治療選択肢としてParadise システムの提供が可能となります。大塚メディカルデバイスと大塚製薬は、共同プロモーション体制のもと、大塚製薬がこれまで培ってきた循環器・腎領域での知見を活かし、患者さんの病態に応じた適切な治療選択肢を届けてまいります。本システムによる治療は、『腎デナベーションシステムの適正使用指針』にて定義された患者さんへ提供されます。
特定非営利活動法人 日本高血圧学会理事長、および自治医科大学内科学講座循環器内科学部門 苅尾七臣教授は、「治療抵抗性高血圧症は、脳心血管疾患や腎不全などの重大な合併症につながるリスクが極めて高い疾患です。保険適用により、必要な患者さんに適切な治療機会を提供できるようになったことは、大きな前進です。また、日本高血圧学会、日本心血管インターベンション治療学会、日本循環器学会が策定した『腎デナベーションシステムの適正使用指針』に従い、治療実施施設要件ならびに適用患者要件を遵守し、適正かつ安全な治療が行われるよう、3学会で協力して取り組んでまいります」とコメントを寄せています。
大塚ホールディングス株式会社 代表取締役社長 兼 CEO、大塚製薬株式会社 代表取締役社長 井上眞は、「治療抵抗性高血圧という医療課題に対し、大塚グループの医療関連事業で培ってきたノウハウを活かし、新たな選択肢を提供できることをうれしく思います。今後も、大塚グループの総力を結集し、患者さんや生活者にとって最適なソリューションを届け、一人ひとりのトータルヘルスケアに貢献すべく取り組んでまいります」と述べています。
大塚メディカルデバイス 代表取締役社長 東條紀子は、「Paradise システムは、2023年に米国食品医薬品局(FDA)から承認を取得しました※。今回の保険適用により、日本の治療抵抗性高血圧症の患者さんが、保険の範囲で新しい治療選択肢にアクセスできるようになったことを大変喜ばしく思います。この治療を必要な患者さんに確実に届けるための仕組みを大塚製薬とともに構築し、今後も当社は、患者さんの健康と医療への貢献に尽力してまいります」と語っています。
大塚メディカルデバイスと大塚製薬では、“Otsuka-people creating new products for better health worldwide”の企業理念のもと、未充足の医療ニーズに新たな価値を提供すべく、引き続き全力で取り組んでまいります。
※米国では、生活習慣改善や薬物療法を行っているにもかかわらず十分に血圧コントロールができない場合の併用治療選択肢として位置づけられ、2023年11月にFDAより承認を取得
| 【製品概要】 |
|
| 販売名 |
Paradise システム |
| 一般的名称 |
腎神経焼灼術用カテーテル |
| 承認番号 |
30700BZX00199000 |
| 使用目的 |
本品は、高血圧治療ガイドラインに従った治療(生活習慣の修正、非薬物療法及び薬物療法)で適切に血圧がコントロールできない治療抵抗性高血圧症患者の追加的治療として血圧を低下させるために使用する。 |
| 製造販売業者 |
大塚メディカルデバイス株式会社 |
| 開発元 |
Recor Medical, Inc. |
| 【保険適用情報】 |
||
| 製品名 |
Paradise カテーテル |
Paradise カートリッジ、 |
| 区分 |
C2(新機能・新技術) |
|
| 適用開始日 |
2026年3月1日 |
|
| 償還価格 |
694,000円 |
124,000円 |
| 準用技術料※1 |
腎血管性高血圧症手術(経皮的腎血管拡張術) 31,840点 |
|
| 留意事項 |
1回の手術に対して2個を限度として算定できる。ただし、医学的必要性から3個以上使用する必要がある場合は、その理由を診療報酬明細書の摘要欄に記載した上で、3個を限度として算定できる。 |
カートリッジは1回の手術に対して1個を限度として算定できる。冷却水の費用は本区分の材料価格に含まれる。 |
| ※1:手術料 |
||
大塚メディカルデバイス
https://www.omd.otsuka.com/
Recor Medical
http://www.recormedical.com/
大塚製薬
https://www.otsuka.co.jp/
businesswire.comでソースバージョンを見る:https://www.businesswire.com/news/home/20260301067557/ja/
Contacts
【お問い合わせ先】
お問い合わせフォーム
報道関係からのお問い合わせ:
コーポレートコミュニケーション部 電話:03-6361-7459
Source: Otsuka Medical Devices Co., Ltd.
本プレスリリースは発表元が入力した原稿をそのまま掲載しております。また、プレスリリースへのお問い合わせは発表元に直接お願いいたします。
このプレスリリースには、報道機関向けの情報があります。
プレス会員登録を行うと、広報担当者の連絡先や、イベント・記者会見の情報など、報道機関だけに公開する情報が閲覧できるようになります。